Молекулярна фізика. Властивості тіл в різних агрегатних станах.
Агрегатні стани речовини (від лат. Aggrego - приєдную) - це стани одного і того ж речовини в різних інтервалах (проміжках) температур і тисків .
Агрегатними станами прийнято вважати газоподібне, рідке і тверде. Найпростішими прикладами існування одного і того ж речовини в цих трьох агрегатних станах, які спостерігаються в повсякденному житті, є лід, вода і водяний пар . Невидимий водяна пара завжди присутній і в навколишньому нас повітрі. Вода існує в інтервалі температур від 0 ° С до 100 ° С, лід - при температурі нижче 0 ° С. При температурі вище 100 ºС і нормальному атмосферному тиску молекули води існують тільки в газоподібному стані - у вигляді водяної пари. Вода, лід і водяна пара - це одне і те ж речовина з хімічною формулою Н2О.
Багато речовин в повсякденному житті ми спостерігаємо тільки в одному з агрегатних станів. так, кисень в навколишньому повітрі є газ. Але при температурі -193 ° С він перетворюється в рідину. Охолодивши цю рідину до -219 ° С, ми отримаємо твердий кисень. І навпаки, залізо в звичайних умовах тверде. Однак при температурі тисяча п'ятсот тридцять п'ять ° С залізо плавиться і перетворюється в рідину. Над розплавленим залізом буде знаходитися газ - пар з атомів заліза.
Різні агрегатні стани існують у кожного речовини. Відрізняються ці речовини не молекулами, а тим, як ці молекули розташовані і як рухаються. Розташування молекул води в трьох агрегатних станах показано на малюнку:

Перехід з одного агрегатного стану в інше. При певних умовах речовини можуть переходити з одного агрегатного стану в інше. Всі можливі при цьому перетворення відображені на малюнку:
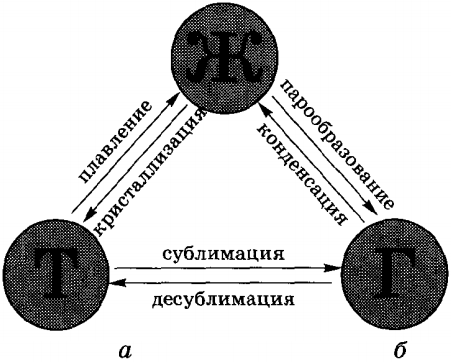
Всього розрізняють шість процесів, при яких відбуваються агрегатні перетворення речовини. Перехід речовини з твердого (кристалічного) стану в рідке називається плавленням, зворотний процес називається кристалізацією , Або ненням. Приклад плавлення - танення льоду, зворотний процес відбувається при замерзанні води.
Перехід речовини з рідкого стану в газоподібний називається паротворенням, зворотний процес називається конденсацією . Приклад пароутворення - випаровування води, зворотний процес можна спостерігати при випаданні роси.
Перехід речовини з твердого стану відразу в газоподібний (минаючи рідкий) називається сублімацією, або сублімацією, зворотний процес називається десублімації. Наприклад, графіт можна нагріти до тисячі, дві тисячі і навіть трьох тисяч градусів і, тим не менш, в рідину він не перетвориться: він буде сублімувати, т. Е. З твердого стану відразу переходити в газоподібний. Безпосередньо в газоподібний стан (минаючи рідкий) переходить і так званий сухий лід (твердий оксид вуглецю СО2), який можна побачити в контейнерах для транспортування морозива. Всі запахи, якими володіють тверді тіла (наприклад, нафталін), також обумовлені сублімацією: вилітаючи з твердого тіла, молекули утворюють над ним газ (або пар), що володіє запахом.
Прикладом десублімації є утворення на вікнах взимку візерунків з кристаликів льоду. Ці красиві візерунки утворюються при десублімації водяної пари, що знаходиться в повітрі.
Переходи речовини з одного агрегатного стану в інше відіграють важливу роль не тільки в природі, а й у техніці. Так, воду, перетворену в пар, можна використовувати а парових турбінах на електростанціях. З розплавлених металів на заводах отримують різні сплави: сталь, чавун, латунь і т. Д. Для розуміння цих процесів треба знати, що відбувається з речовиною при зміні його агрегатного стану і за яких умов це зміна можлива.




